HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > 高知-フュルスナーカップリング
高知-フュルスナーカップリングとは
高知-フュルスナーカップリングとは、鉄触媒存在下で、芳香族またはビニルハロゲン化物R-Xと脂肪族または芳香族グリニャール試薬R’-MgX’とから炭素-炭素カップリング体R-R’を得るクロスカップリング反応であり、1971年に、高知らの研究グループによって報告された(i)。
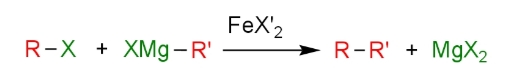
コーリー-ハウス-ポスナー-ホワイトサイズ反応では有機リチウムから調整したクプラートを用いていたのに対し、本反応ではグリニャール試薬が用いられており、類似した反応である。
反応機構
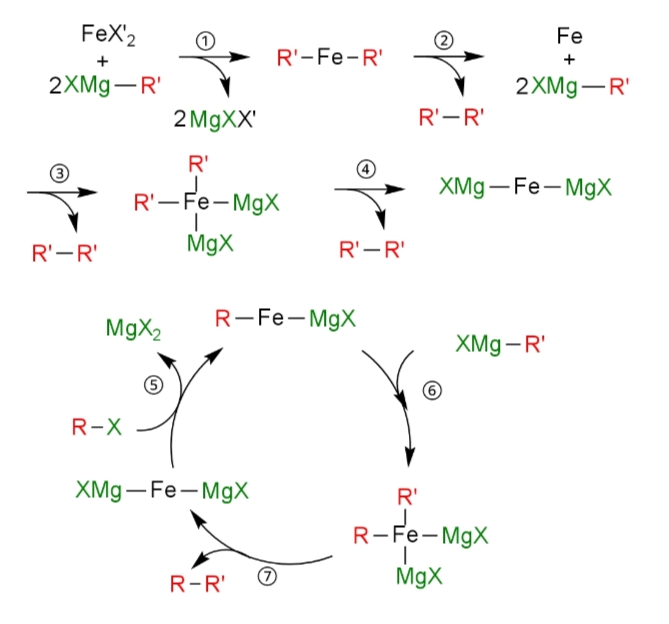
①トランスメタル化
グリニャール試薬R’-MgX’の炭素基R’が鉄錯体上の配位子と交換してトランスメタル化する。
②還元的脱離
R’-R’の還元的脱離によって鉄が0価に還元される。
③酸化的付加
グリニャール試薬の酸化的付加によって有機鉄錯体が形成される。
④還元的脱離
再度、R’-R’の還元的脱離によって鉄アート錯体が生成する。
⑤酸化的付加
次に、酸化的付加によって鉄触媒がハロゲン化物のR-X結合に挿入されて、有機鉄錯体が形成される。
⑥トランスメタル化
グリニャール試薬R’-MgX’の炭素基R’が有機鉄錯体上の配位子と交換してトランスメタル化する。
⑦還元的脱離
最後に、還元的脱離によって炭素-炭素結合R-R’が生成する。
適用範囲
ハロゲン化試薬R-X
ハロゲン化アリールやハロゲン化アルケニルを用いることができ、塩化物やトシラート、トリフラートを用いることができる。ヨウ化物および臭化物では脱ハロゲン化が優先的に進行する。
ハロゲン化アルキルを用いた際、β水素の存在によって脱離反応が競合するため、一般的に収率は低い。しかし、配位子や添加剤を加えることによって、ハロゲン化アルキルも用いることができる(後述)。
グリニャール試薬R’-MgX’
アルキルグリニャール試薬はβ水素脱離を起こさないため、アリールグリニャール試薬だけでなくアルキルグリニャール試薬も用いることができ、様々な構造のものが使用できる。
触媒
2価の鉄触媒としてはFeCl2やFe(OAc)2、FeCl2(dppp)、FeCl2(dppy)などが、3価の鉄触媒としてはFeCl3やFeBr3、FeF3、Fe(acac)3などが用いられる。また、NHC配位子が配位した鉄触媒も用いられる。
溶媒
グリニャール試薬はプロトン性溶媒と反応するため、溶媒としては、グリニャール試薬を安定化させる効果もあるTHFやジエチルエーテルなどのエーテル系溶媒が用いられる。遷移金属触媒は空気や水分に敏感なため、溶媒は脱水&脱気条件である必要あり。
反応条件
脱水&脱気条件で行なう。
前身の反応
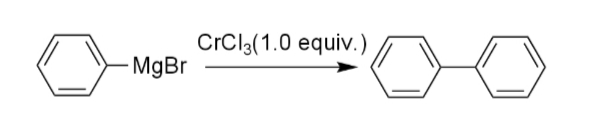
古くから、グリニャール試薬を用いるカップリングは知られていたが、化学量論的な金属塩を必要としていた。例えば、1914年にターナーはグリニャール試薬のホモカップリング反応を報告したが、化学量論量の塩化クロム(III)を必要としていた。また、ギルマンは同様の反応が塩化ニッケル(II)、塩化コバルト(II)、塩化銀(I)を用いた際にも進行することを報告していた(iii)。
また、1940年代にカラッシュはグリニャール試薬とハロゲン化アリールまたはハロゲン化ビニルを用いた塩化コバルト(II)触媒存在下におけるクロスカップリング(iv)、1971年に高知らは銀触媒存在下におけるクロスカップリング(v)を報告した。
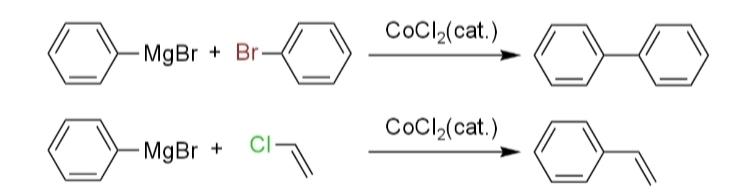
しかし、どちらの反応もラジカル的に進行し、ホモカップリング体の形成によって収率は高くなかった。
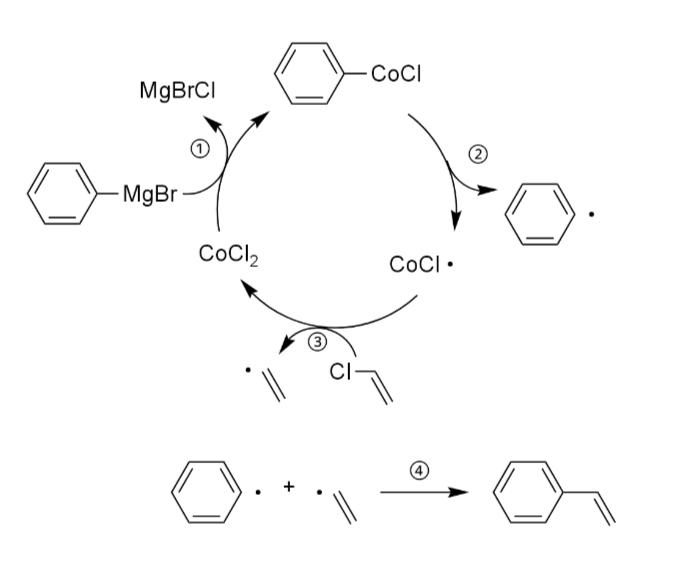
一方、同年の1971年に高知らは、銅触媒(vi)や鉄触媒(i)を用いた本反応でクロスカップリング体が多く得られたことを確認し、それらの反応機構はラジカル的に進行しているとは考えられず、近代的なクロスカップリング反応の先駆けとなった。
応用例
ハロゲン化アルキルへの応用
通常、パラジウムやニッケル触媒を用いた反応でハロゲン化アルキルを用いるとβ水素脱離が優先的に起こってしまう。
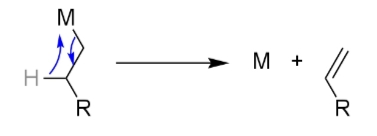
本反応も例外ではないが、2004年にフュルスナーらのグループ(vii)と中村らのグループ(viii)がTMEDA(テトラメチルエチレンジアミン)を系内に存在させることによって、ハロゲン化アルキルでもβ脱離を抑え収率良く本反応が進行することを報告した。
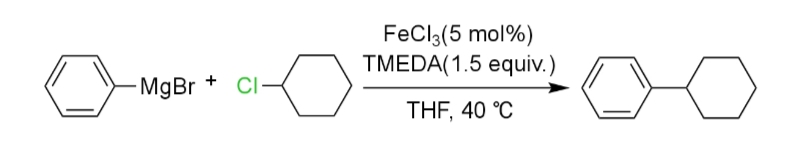
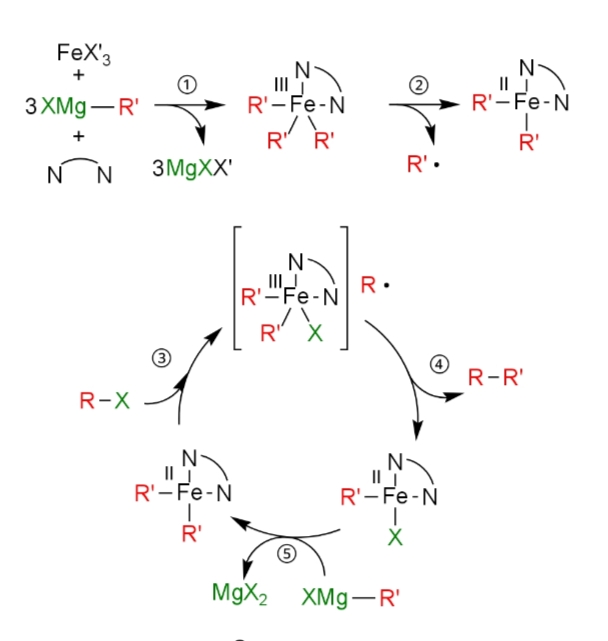
反応機構(ix)としては、初めに鉄原子にTMEDAが配位子してグリニャール試薬とトランスメタル化し(①)、ラジカルを発生させながらグリニャール試薬由来のアリール基R’2つとTMEDAが四面体構造となるように配位した有機鉄錯体が生じる(②)。次に、有機鉄錯体がハロゲン化アルキルR-Xをラジカル開裂させ、ジアリールハロゲン化鉄(III)とアルキルラジカルが生じる(③)。このとき、アルキルラジカルが鉄原子に配位せず、配位したとしても6配位となって空の配位点がないため、β水素脱離は進行しない。そして、アリール基とアルキルラジカルの間に炭素-炭素結合が生成してクロスカップリング体が得られ(④)、最後にグリニャール試薬と有機鉄錯体とがトランスメタル化して鉄触媒が再生する(⑤)。
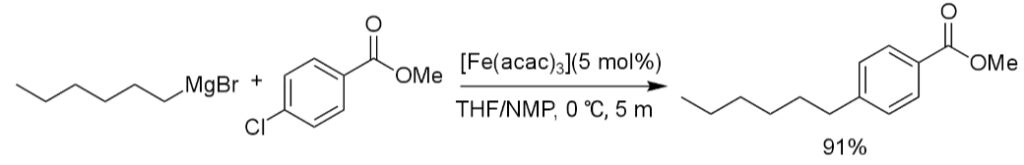
これらの反応は進行が早く、グリニャール試薬と反応するエステル、ケトン、イソシアネート、ニトリルを持つ基質においても本反応は進行する(vii)(viii)。
TMEDAはマグネシウムにも配位するため、1当量以上加える。
NMPの添加
NMPやNBPを添加すると反応性が上がり、基質適用範囲が広がる(x)。これは、系内で発生するアニオン[Fe8R12]– とマグネシウムカチオンとによるクラスターをNMPは崩す役割があり、それによって反応を活性化させる(xi)。
ワンポット合成
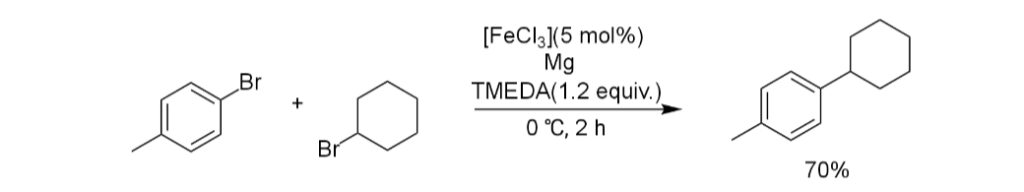
2009年にウォンゲリンらによって、ハロゲン化アリールとハロゲン化アルキル、マグネシウムの混合物に、5mol%の塩化鉄と1.2当量のTMEDAを加えることによって、グリニャール試薬を系内で調整すると同時に本反応を進行させられることが報告された(xii)。
実験手順
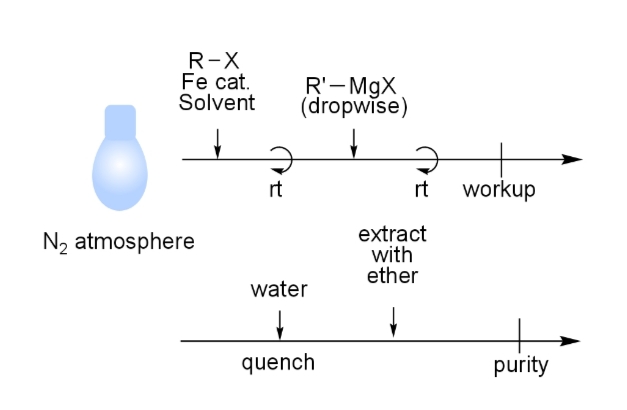
反応例
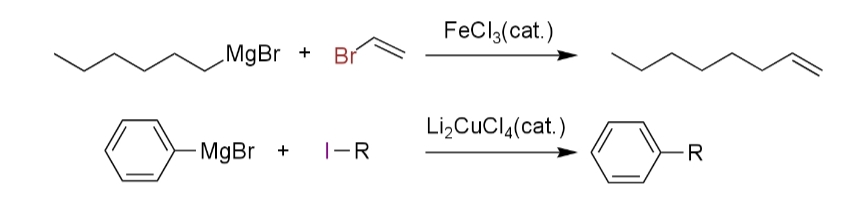
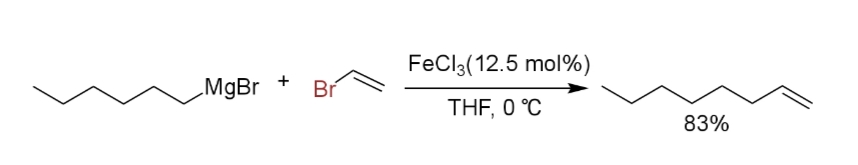
ヘキシルグリニャール試薬と臭化ビニルを反応させると1-オクテンが得られる(i)。
参考文献
(i) Tamura, M.; Kochi, J. K. J. Am. Chem. Soc. 1971, 93, 1487–1489.
(ii) Dahadha, A. A.; Aldhoun, M. M.; Hassan, M.; Ibrahim Q. A.; Talat, N. T. Org. Commun. 2021, 14, 1-38.
(iii) Gilman H. J. Am. Chem. Soc.1939,61 957-959.
(iv)Kharasch, M. S.; Fields, E. K. J. Am. Chem. Soc. 1941, 63, 2316–2320.
(v)Kochi, J. K.; Tamura. M. J. Am. Chem. Soc. 1971, 93, 1483–1485.
(vi) Kochi, J. K.; Tamura, M. J. Am. Chem. Soc. 1971, 93, 1485–1487.
(vii) Martin, R.; Fürstner, A.; Angew. Chem. Int. Ed. 2004, 43, 3955.
(viii) Nakamura, M.; Matsuo, K.; Ito, S.; Nakamura, E. J. Am. Chem. Soc. 2004, 126, 3686.
(ix) Noda, D.; Sunada, Y.; Hatakeyama, T.; Nakamura, M.; Nagashima, H. J. Am. Chem. Soc. 2009, 131, 6078–6079.
(x) Fürstner, A.; Leitner, A. Angew. Chem. Int. Ed. 2002, 41, 609.
(xi) Muñoz, S. B.; Daifuku, S. L.; Sears, J. D.; Baker, T. M.; Carpenter, S. H.; Brennessel, W. W.; Neidig, M. L. Angew. Chem., Int. Ed. 2018, 57, 6496– 6500.
(xii) Czaplik, W. M.; Mayer, M.; von Wangelin, A. J. Angew. Chem. Int. Ed. 2009, 48, 607.
HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > 高知-フュルスナーカップリング
