HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > ゴンバーグ-バックマン反応
ゴンバーグ-バックマン反応とは
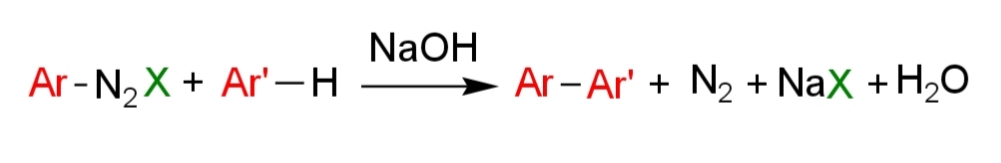
ゴンバーグ-バックマン反応とは、ジアゾニウムアリール化合物Ar-N2Xとアリール化合物Ar’-Hを用いてジアリールAr-Ar’を得るクロスカップリング反応であり、モーゼ・ゴンバーグとワーナー・バックマンによって発見された(i)。
Ar-N2 X+ Ar‘−H → Ar−Ar’
反応機構
「ゴンバーグ-バックマン反応の反応機構」「gomberg-bachmann-reaction-mechanism」
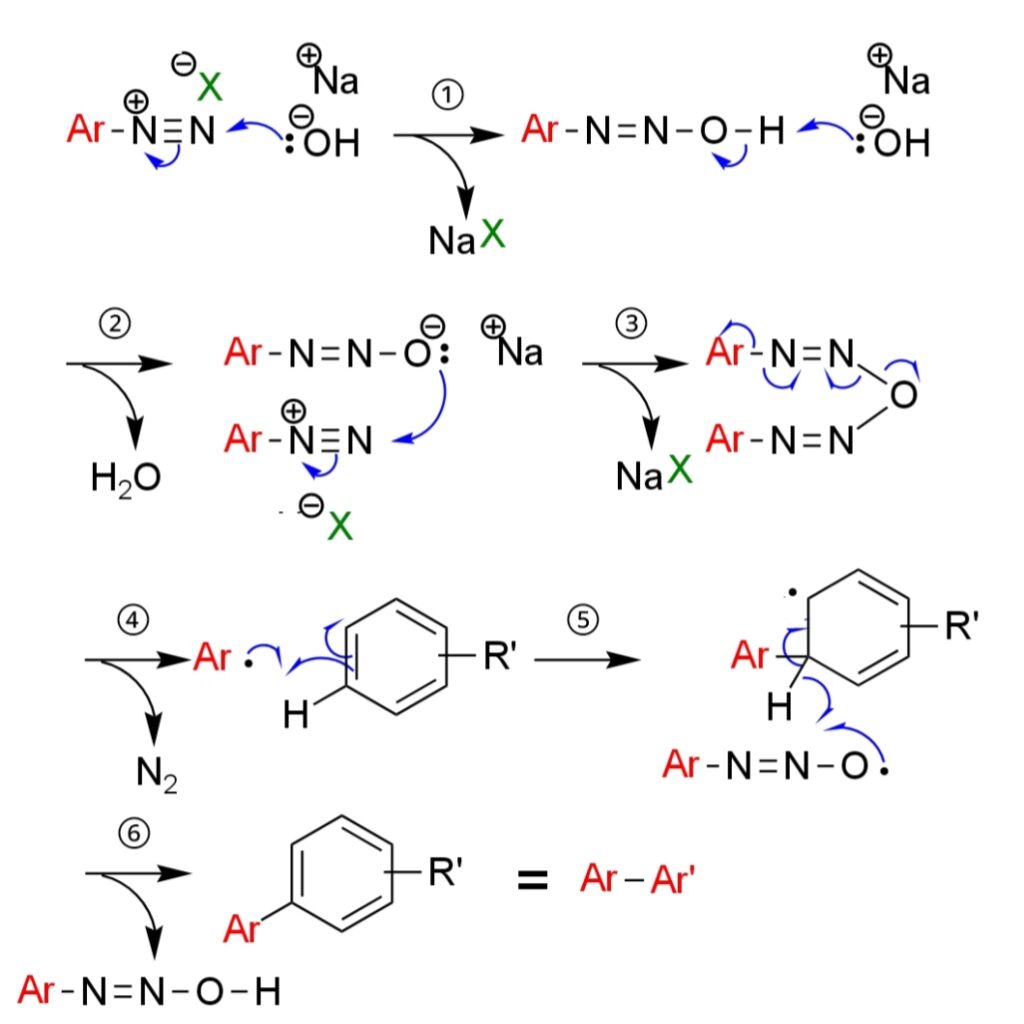
①ラジカル開裂
初めに、芳香族ジアゾニウム塩と水酸化ナトリウムが反応し、ジアゾヒドロキシドAr-N=N-OHが生じる。
②酸塩基反応
ジアゾヒドロキシドAr-N=N-OHのプロトンを水酸化ナトリウムが引き抜き、ジアゾタートAr-N=N-O–が生成する。
③求核攻撃
ジアゾタートAr-N=N-O–がもう一分子のジアゾニウム塩に求核攻撃をする。
④ラジカル開裂反応
窒素分子を発生させながら、ラジカル開裂し、アリールラジカルが生じる。
⑤ラジカル付加反応
アリールラジカルがアリール化合物Ar-Hがもう一分子の芳香族化合物に付加する。
⑥ラジカル引き抜き反応
ラジカルが水素ラジカルを引き抜き、反応が完了する。
副反応
アリール同士の結合箇所が異なる構造異性体が生じる。また、電子豊富なアリール化合物を用いると、ジアゾカップリングが副反応として起こる可能性がある。さらには、ジアゾニウム塩から生じるアリールラジカルAr・がホモカップリングしてジアリール体Ar-Arを生じる可能性もある。ジアゾニウム塩は反応性が高く不安定であるため、他にも様々な副反応が起こりやすく、一般的に本反応の収率は低い。
適用範囲
アリールジアゾニウム塩
塩基に耐えられる基質であれば用いることができるため、基質の適用範囲は広い。ジアゾニウム塩は不安定であるため、調整後そのまま反応に用いることが多い。
アリール化合物
塩基に耐えられる基質であれば用いることができるため、基質の適用範囲は広い。ただし、二重結合など、アリールラジカルと反応しやすい官能基があると収率は落ちる。
溶媒
ジアゾニウム塩の調整は水系で行なうことが多く、溶媒には水が使われる。一般的に、ジアゾニウム塩は有機溶媒に難溶である。
反応条件
アリールジアゾニウム塩は不安定であり、温度が高いと速やかに分解して溶媒の水と反応しフェノール体となるため、氷浴下などで反応を行なう。
実験手順
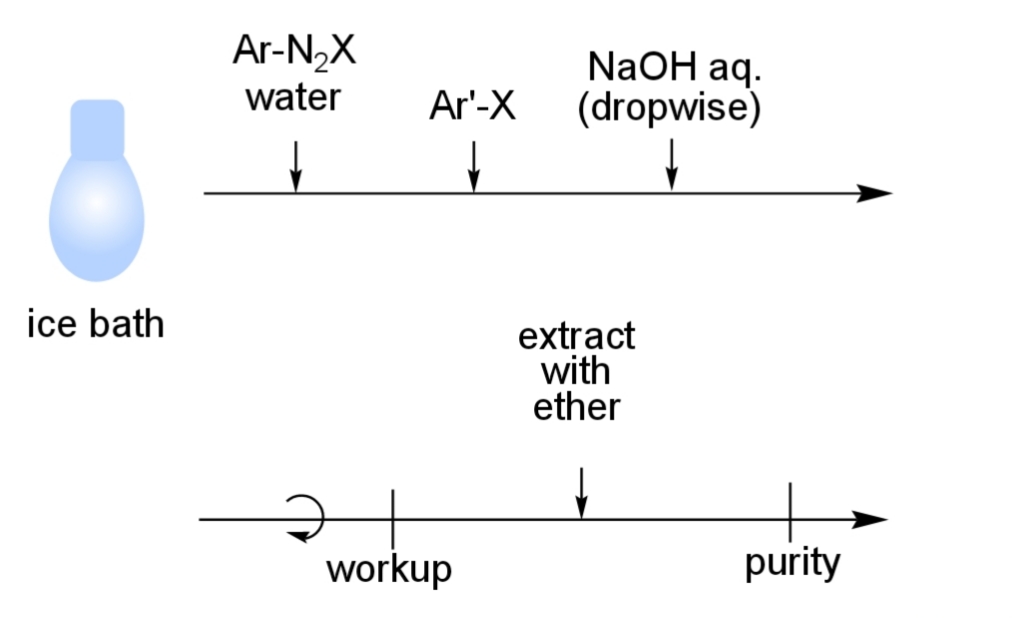
応用例
プショール反応
プショール反応は、ゴンバーグ・バックマン反応を分子内反応に応用した反応であり、銅触媒が用いられる。
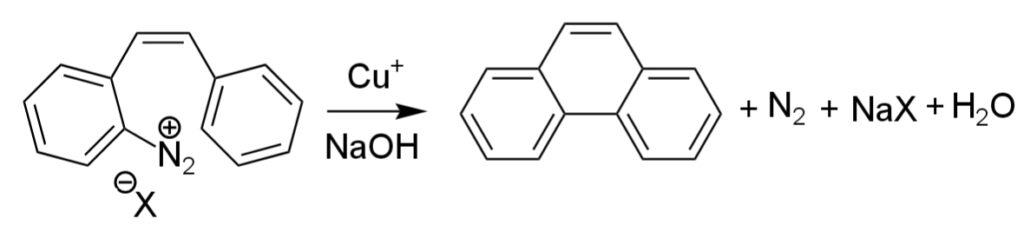
反応機構は次のようになる。
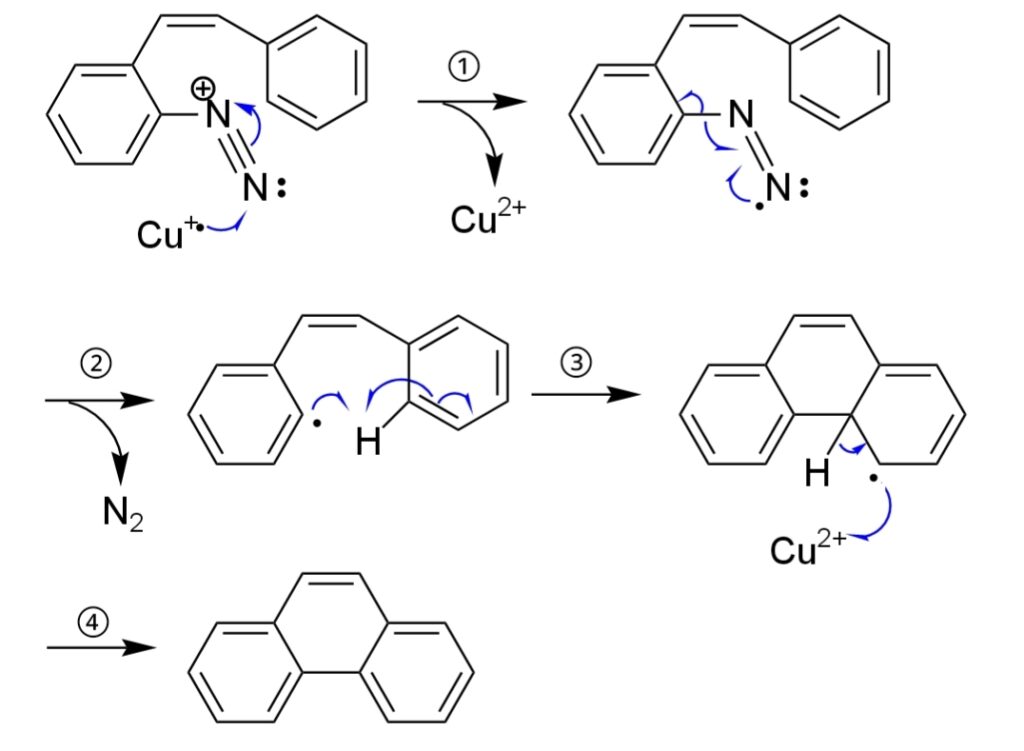
①還元反応
銅塩によってアリールジアゾニウムカチオンが還元される。
②ラジカル開裂反応
窒素分子を発生させながら、ラジカル開裂し、アリールラジカルがしょうじる。
③ラジカル付加反応
アリールラジカルが分子内にあるもう一つの芳香環に付加する。
④1電子移動(SET)
銅塩が電子を受け取って再生し、プロトンが引き抜かれて、反応が完了する。
反応例
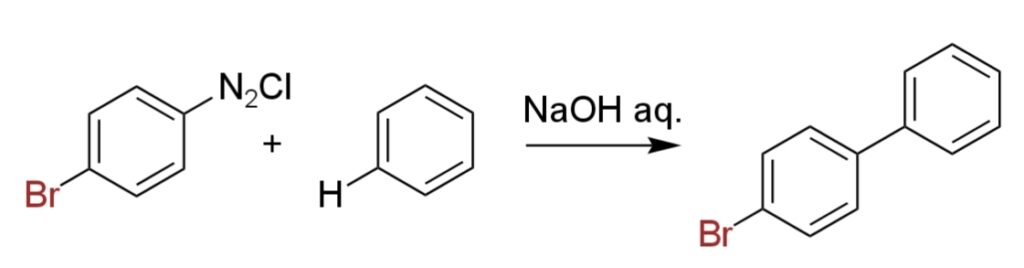
p-ブロモアニリンから作製したジアゾニウム塩とベンゼンを反応させるとp-ブロモビフェニルが得られる(iii)。
関連反応
・ジアゾカップリング
参考文献
(i) Gomberg, M.; Bachmann, W. E. J. Am. Chem. Soc. 1924, 42, 2339–2343.
(ii) Pschorr, R. Chem. Ber. 1896, 29, 496–501.
(iii) Gomberg, M.; Bachmann, W. E. Org. Synth. 1928, 8, 42.
HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > ゴンバーグ-バックマン反応
