HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > カストロ-ステファンズカップリング
カストロ-ステファンズカップリングとは
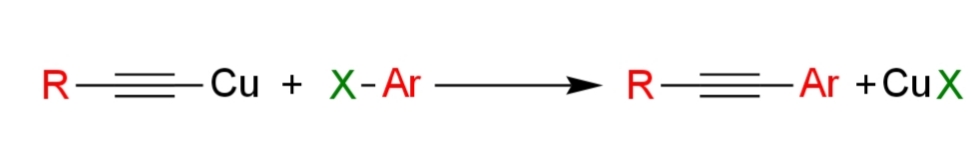
カストロ-ステファンズカップリングとは銅アセチリドR-C三C-Cuとハロゲン化アリールAr-Xから二置換アルキンR-C三C-Arを得るクロスカップリング反応であり、1963年にカストロとステファンズによって発見された(i)。
1973年には、パラジウム触媒の添加およびin-situで銅アセチリドを生成させる薗頭カップリングに改良されている。
反応機構
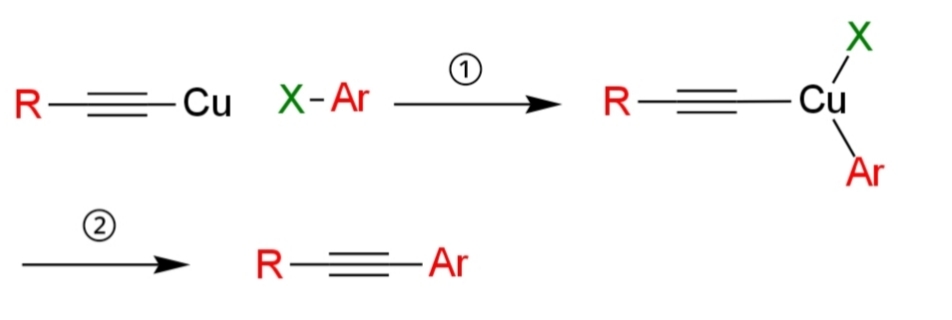
①酸化的付加
銅アセチリドが配位した銅イオンにハロゲン化アリールが酸化的付加する。
②還元的脱離
二置換アルキンR-C三C-Arが還元的脱離しながら、炭素-炭素共有結合が形成され、ホモカップリング反応が完了する。
副反応
酸素などの酸化剤が系内に存在しているとグレーサーカップリングが進行し、アルキンのホモカップリング体が生成する(i)。
適用範囲
銅アセチリドR-C三C-Cu
塩基にある程度耐えられる基質であれば用いることができるため、基質の適用範囲は広い。
ハロゲン化アリールAr -X
塩基にある程度耐えられる基質であれば用いることができるため、基質の適用範囲は広い。
溶媒
多くの場合は塩基としてピリジンが用いられる。
反応条件
グレーサーカップリングを防ぐために脱気条件で行なう(i)。また、パラジウム触媒が存在しない条件では反応速度が遅いため、通常は加熱を行なう。
実験手順
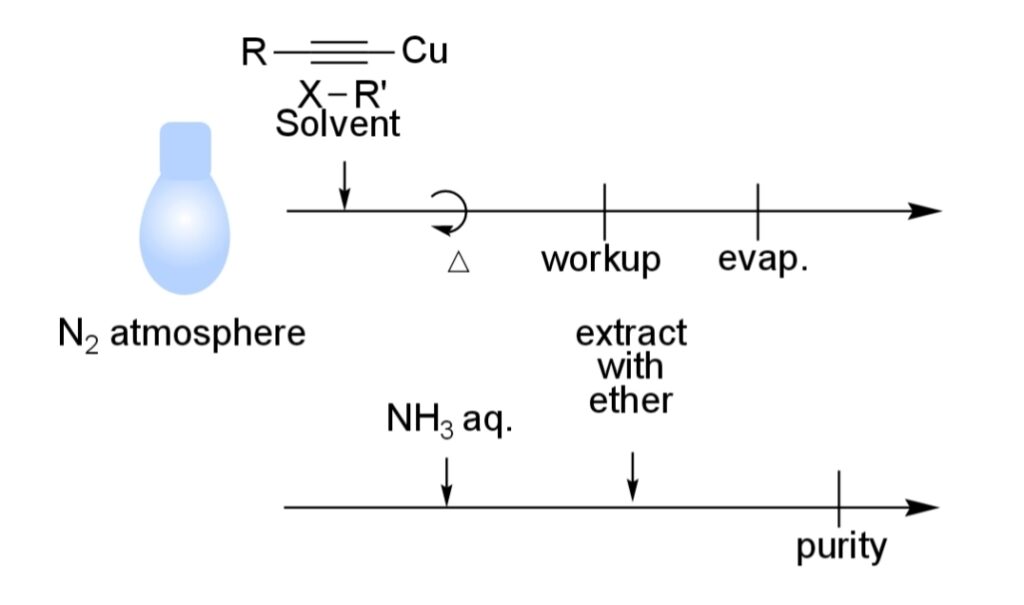
副生成物の銅塩はアンモニア水溶液を加えて水溶性にする。
反応例
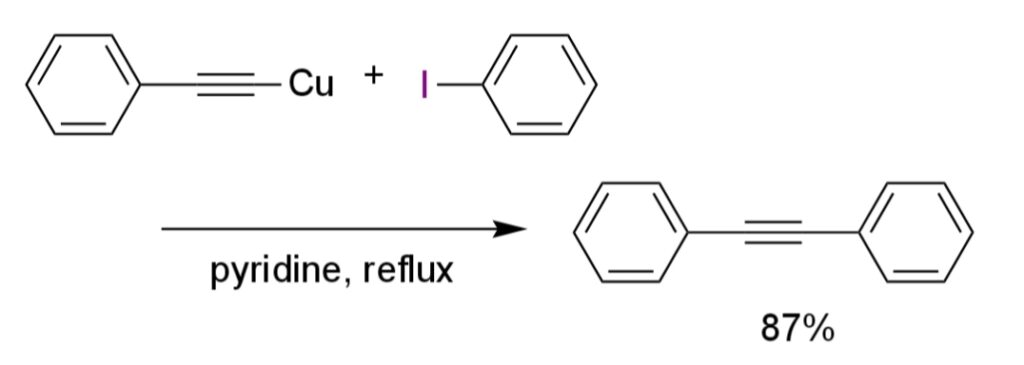
ヨードベンゼンと銅フェニルアセチリドを反応させると、ジフェニルアセチレンが得られる(i)。
関連反応
・薗頭カップリング
参考文献
(i) Stephens, R. D.; Castro, C. E. J. Org. Chem. 1963, 28, 3313 – 3315.
(ii) Owsley, D. C.; Castro, C. E. Org. Synth. 1972, 52,128.
HOME > 有機化学 > クロスカップリング反応(炭素-炭素) > カストロ-ステファンズカップリング
